КОЛЛОИДНЫЙ ЖУРНАЛ, 2015, том 77, № 4, с. 526-529
УДК 541.18
О РОЛИ КОЭФФИЦИЕНТА АКТИВНОСТИ В ПРОЦЕССАХ ДИФФУЗИИ ИОННЫХ ПАВ В МИЦЕЛЛЯРНЫХ РАСТВОРАХ
© 2015 г. А. И. Русанов*, **, Т. Г. Мовчан*, Е. В. Плотникова*
*Институт физической химии и электрохимии им. А.Н. Фрумкина РАН 119071 Москва, Ленинский проспект, 31 **Санкт-Петербургский государственный университет 198504 Санкт-Петербург, Петродворец, Ульяновская ул., 1 E-mail: movchan_tamara@mail.ru Поступила в редакцию 09.02.2015 г.
Сформулированы теоретические соотношения, описывающие влияние коэффициента активности (отражающего взаимодействие между частицами) на коэффициент диффузии ПАВ в мицеллярной системе. С помощью бром-селективного электрода измерен коэффициент активности бромида гек-садецилтриметиламмония в водном мицеллярном растворе. Анализ полученных данных показывает, что в возрастании коэффициента диффузии выше ККМ и последующем его снижении действие подвижности ПАВ и вязкости оказывается сильнее влияния взаимодействия между частицами ми-целлярной системы.
DOI: 10.7868/S0023291215040175
ВВЕДЕНИЕ
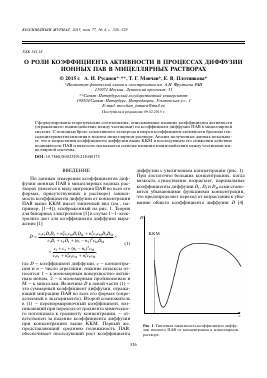
По данным измерения коэффициентов диффузии ионных ПАВ в мицеллярных водных растворах (имеется в виду миграция ПАВ во всех его формах, присутствующих в растворе) зависимость коэффициента диффузии от концентрации ПАВ выше ККМ имеет типичный вид (см., например, [1—4]), изображенный на рис. 1. Теория для бинарных электролитов [5] в случае 1-1-элек-тролита дает для коэффициента диффузии выражение [1]
D — C1C2D1D2 + n2C1CMD1DM + n1C2CMD2DM х C1D1 + C2D2 + (n1 - n2)2 CMDM
v C1 + C2 + (n - n2)2CM
(1)
2
С1С2 + П2 С1СМ + П1 С2СМ
где Б — коэффициент диффузии, с — концентрация и п — число агрегации; нижние индексы относятся: 1 — к мономерным поверхностно-активным ионам, 2 — к мономерным противоионам и М — к мицеллам. Величина Б в левой части (1) — это суммарный коэффициент диффузии, отражающий миграцию ПАВ во всех его формах (определяемый в эксперименте). Второй сомножитель в (1) — перенормировочный коэффициент, возникающий при переходе от градиента химического потенциала к градиенту концентрации, — ответственен за падение коэффициента диффузии при концентрациях выше ККМ. Первый же, представляющий среднюю подвижность ПАВ, обеспечивает последующий рост коэффициента
диффузии с увеличением концентрации (рис. 1). При достаточно больших концентрациях, когда вязкость существенно возрастает, парциальные коэффициенты диффузии Б1, Б2 и Бм сами становятся убывающими функциями концентрации, что предопределяет переход от возрастания к убыванию общего коэффициента диффузии Б [4].
D
Рис. 1. Типичная зависимость коэффициента диффузии ионного ПАВ от концентрации в мицеллярном растворе.
c
Примечательно, что теория [1, 5] диффузионной подвижности ПАВ была сформулирована для идеальной мицеллярной системы и в ее рамках объяснение хода представленной рис. 1 зависимости дается без учета взаимодействия между частицами. Очевидно, однако, что теория не может считаться полной без учета коэффициента активности ПАВ. В работах [2, 3] была попытка использовать коэффициент активности для объяснения возрастания с концентрацией коэффициента диффузии. Как показал дальнейший анализ, проведенное в [2, 3] рассмотрение нуждается в уточнении и дополнении, что и составляет цель данного сообщения.
ТЕОРИЯ
Дуалистическая запись уравнения диффузионного потока ионного ПАВ J (Ь — феноменологический коэффициент неравновесной термодинамики, ц — химический потенциал, Б — коэффициент диффузии и с — концентрация)
J = -ЬУц = -ВУ с (2)
сразу дает связь между коэффициентом диффузии Б и подвижностью ПАВ Г = Ь/с в виде [1—3]
(а)
(б)
D = Г-^-
д ln c
(3)
Разделив производную на идеальную и неидеальную части, представим (3) в виде
D = L
) +VRT^ д ln cj id д ln c.
(4)
где V — общее число ионов, образующихся при диссоциации одной молекулы ПАВ (для 1-1-элек-тролита V = 2), Я — газовая постоянная, Т — температура и /± — средний коэффициент активности электролита. Поскольку мицеллообразование само по себе связано с отклонением от идеальности, мы должны оговориться, что под идеальностью при рассмотрении первого слагаемого в квадратных скобках (4) понимается отсутствие любых взаимодействий в системе, включающей мономеры и мицеллы, а не отсутствие мицелл. Иными словами, агрегативная часть коэффициента активности [2, 3] включена здесь в первое слагаемое. Именно это слагаемое уже было рассчитано и представлено в формуле (1) вторым сомножителем. Таким образом, выражение (4) четко указывает место поправки, связанной с коэффициентом активности. Отметим, что в мицеллярной системе средний коэффициент активности электролита может быть выражен через парциальные коэффициенты активности мономеров и мицелл и также связан с характеристиками агрегации. Соответствующие формулы даны в [6], но нас сейчас интересует классический вид среднего коэффициента активности (как бы в отсут-
Рис. 2. Типичный вид зависимости lnf± от c (а) и lnc (б).
ствие агрегации), поскольку именно так он определяется из опыта.
В соответствии с (4) поправка к коэффициенту диффузии, связанная с коэффициентом активности, имеет вид
D± = vRTL
■ д ln f±, д ln c
а ее производная дается выражением
dD д ln c
= v RT
dL д ln f± д ln c д ln c
+ L
■ д 2ln f±л
(5)
(6)
5(ln c)2
Установление зависимости среднего коэффициента активности электролита от концентрации — это классическая задача электрохимии. Огромный экспериментальный материал в этой области свидетельствует, что для сильных электролитов кривая зависимости f± и lnf± от концентрации характеризуется наличием минимума [7]. Для большинства галогенидов щелочных металлов координата минимума близка к с ~ 0.5 М [8]. При c > 5 М величина lnf линейно возрастает с lnc. В случае 1-1-электролитов с более сложной структурой ионов положение минимума и начало линейного роста коэффициента активности сдвигается в область меньших концентраций. Нужно отметить, что в области малых концентраций ход зависимостей lnf± от c и lnc принципиально различен. В первом случае при c ^ 0 имеем предельное значение производной д ln fj dc = -да в соответствии с теорией Дебая—Хюккеля (рис. 2а). При переходе к логарифмическому масштабу концентрации точка нулевой концентрация электролита уходит в отрицательную бесконечность, и кривая lnf± уже не может пересекать ось абсцисс, а лишь асимптотически к ней приближается. При этом кривизна кривой меняет знак, и на ней появляется точка перегиба (рис. 2б). Чтобы учесть все это в нашем анализе, необходимо ответить на два вопроса: применимы ли эти общие
0
528
РУСАНОВ и др.
1п(Я/Аз) 1п(п/По) 2
3 Ш □ □
-8 1п с [М]
Рис. 3. Концентрационная зависимость среднего коэффициента активности /± (1), относительных вязкости 1п(п/ло) (2) и коэффициента диффузии 1п(_0/До) (3) в растворах бромида гексадецилтриметиламмония при 30°С в логарифмических координатах: А — ККМ, Б — точка перегиба, В — точка минимума.
представления к ПАВ и мицеллярным системам и где, по отношению к точке перегиба, располагается ККМ? Ответ на эти вопросы дает проведенный нами эксперимент.
ЭКСПЕРИМЕНТ И ОБСУЖДЕНИЕ
Для опытов был выбран уже исследованный в отношении коэффициента диффузии [2, 3] бромид гексадецилтриметиламмония, который, как и любая соль, является сильным электролитом и, к тому же, 1-1-электролитом, к которому применима формула (1). Препарат фирмы ACROS OR-GANICS с содержанием 99% чистого вещества дополнительной очистке не подвергали. Для приготовления растворов использовали дистиллированную воду с удельной электропроводностью не выше 2 х 10—6 Ом-1 см-1. Интервал исследуемых брутто-концентраций бромида гексадецилтриметиламмония составлял 0.0005—0.27 М.
Среднюю активность а бромида гексадецилт-риметиламмония в водном растворе определяли потенциометрическим методом, используя бром-селективный электрод (ЭКОМ) и хлорсеребря-ный электрод сравнения (ЭВ1-1М3.1.), на основе
данных о потенциале Е измерительной ячейки, предварительно прокалиброванной по стандартным растворам КВг. Расчет вели по уравнению
Е = Ео + Б
(7)
где Е0 — значение потенциала в начальной точке диапазона калибровочной кривой, Б — коэффициент наклона электродной функции, а0 — активность фонового электролита (воды). Измерения проводили с помощью ионометрического преобразователя ЭКОТЕСТ-120 (с пределом допускаемой абсолютной погрешности ±0.005 мВ) в совокупности с автоматическим коммутатором КМ-8, обеспечивающим переключение каналов фиксирования потенциала измерительной ячейки и температуры исследуемого раствора. Результаты эксперимента записывались автоматически с интервалом в 1 с. Измерения проводили при температуре 30°С (использовали термостат ТЖ-ТС-01) с точностью ±0.1°С. Ошибки определения средней активности не превышали 5%.
Полученная кривая зависимости 1п/± от 1п с показана на рис. 3 (кривая 1). Очевидно, что она соответствует кривой, приведенной на рис. 2б.
а
а
о
Точка перегиба располагается при c = 0.002 М, а минимум отвечает концентрации c = 0.05 М. Значение ККМ, полученное при 30°C методом электропроводности, составило cm = 0.001 М (lncm = -6.9), что близко к литературным значениям [9]. Заметим, что появление точки перегиба на кривой зависимости от концентрации среднего коэффициента активности ионного ПАВ никак не связано с мицеллообразованием (см. рис. 2). По этой причине взаимное положение точки перегиба и координаты ККМ ничем не обусловлено (на рис. 3 точка перегиба лежит правее ККМ). В качестве дополнения на рис. 3 приведены полученные ранее концентрационные зависимости коэффициента диффузии бромида гексадецилтриметил-аммония и относительной вязкости его водного раствора [2].
Обращаясь теперь к формуле (6), мы можем сказать, что в районе ККМ дГ/д lnc > 0,
д ln fjд ln c < 0 и д2lnfjd(ln c)2 < 0, что делает всю производную (6) отрицательной. Это значит, что отклонение коэффициента активности от единицы работает на понижение коэффициента диффузии, вместе со вторым сомножителем формулы (1) Правее минимума на кривой 1 (рис. 3) мы имеем обратную ситуацию, но рост коэффициента диффузии начинается уже с концентрации, весьма бли
Для дальнейшего прочтения статьи необходимо приобрести полный текст. Статьи высылаются в формате PDF на указанную при оплате почту. Время доставки составляет менее 10 минут. Стоимость одной статьи — 150 рублей.