ЖУРНАЛ ФИЗИЧЕСКОЙ ХИМИИ, 2015, том 89, № 2, с. 354-356
КРАТКИЕ СООБЩЕНИЯ
УДК 541.8.127: 519. 24/27
СТЕХИОМЕТРИЯ СМЕШАННО-ЛИГАНДНОГО КОМПЛЕКСА ГЕПАРИН—Си2+—ГЛИЦИН ПО ДАННЫМ ДИФФЕРЕНЦИАЛЬНО-ТЕРМИЧЕСКОГО АНАЛИЗА И ИК-СПЕКТРОСКОПИИ
© 2015 г. М. А. Феофанова, Ю. В. Францева, Е. В. Журавлев, Н. В. Баранова, С. С. Рясенский
Тверской государственный университет E-mail: m000371@tversu.ru Поступила в редакцию 27.05.2014 г.
Предложена методика синтеза, выделения и очистки смешанно-лигандного комплекса гепарина с катионами меди и глицином. Проведено комплексное физико-химическое исследование комплекса методами элементного, термического и спектрального анализа. Определен элементный и кри-сталлогидратный состав комплекса, предложена брутто-формула комплекса: Na3CuHepGly • 2H2O.
Ключевые слова: гепарин, ион меди, глицин. DOI: 10.7868/S0044453715020090
Широкое распространение в медицинской практике за последние годы получил гепарин (Hep) как нетоксичный и эффективный антикоагулянт. В силу своих структурных особенностей, а именно большого количества донорных центров: карбоксильной группы, сульфогруппы, гидроксо-группы, гликозидного и эфирного кислорода и амидного азота (рис. 1) гепарин способен взаимодействовать как с катионами различных металлов, так и с низкомолекулярными биологически активными веществами [1—4].
Структурная формула мономерного звена гепарина приведена ниже:
oso3h
Ch2
-UN
oso3h
nhso3h
Из ряда катионов металлов нами был выбран ион меди, который входит в состав многих важнейших ферментов, присутствует в системе антиокси-дантной защиты организма, связывает микробные токсины и усиливает действие антибиотиков, обладает выраженным противовоспалительным действием, необходим для регулирования процессов снабжения клеток кислородом. Кроме того, система ион меди—гепарин была изучена нами ранее [3], для нее был идентифицирован следующий набор высокой устойчивости комплексных форм СиНер2-, СиОННер3-, Си(ОН)2Нер4. В каче-
стве низкомолекулярного биологически активного вещества нами был взят глицин (МН2—СН2— СООН), который является исходным материалом для синтеза аминокислот и применяется в медицине для регуляции обменных функций организма и нормализации процессов возбуждения и торможения в центральной нервной системе [5]. Химические равновесия в системе гепарин — глицин (01у), исследованные ранее [6], идентифицировали ряд
комплексных форм HepGly7 , H2HepGly5 и
5-
H3HepGly4 . В физиологическом интервале рН
Поглощение
0.7
0.6
0.5
3500
2500
1500
500
V, см
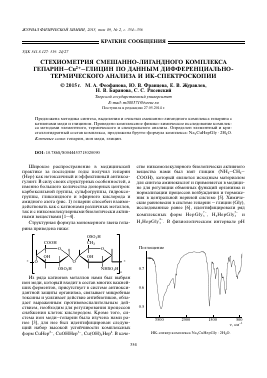
ИК-спектр комплекса Na3CuHepGly • 2H2O.
*
*
СТЕХИОМЕТРИЯ СМЕШАННО-ЛИГАНДНОГО КОМПЛЕКСА 355
Результаты ИК-спектроскопического анализа комплекса Na3CuHepGly • 2H2O
Образец VN—H vO—H VC—H vas CO (COO-) vs CO (COO) vas S=O vs S=O vas C-O-C vsC-O-C
Гепарин Комплекс 3500-3300 3500-3300 3400 3300 3000-2840 3000-2800 17 1610 50 1430 1415-1380 1410-1390 1230 1195-1185 1160-1075 1150-1080 1135 1135
(6.80 < рН < 7.40) доминирует протонированная форма H3HepGly ^.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для проведения синтеза использовали стандартный фармакологический раствор высокомолекулярного гепарина производства "Московский эндокринный завод", упакованный во флакон по 5 мл. Каждый миллилитр такого раствора содержит 5000 ЕД, каждая единица соответствует 0.0077 мг гепарина.
Раствор хлорида меди готовили из соответствующей соли с последующей стандартизацией раствора методом комплексонометрического титрования. Глицин имел квалификацию "ч.д.а.". Термический анализ проводили на дифференциальном сканирующем калориметре NETZSCH STA 449F3, элементный анализ — на элементном анализаторе CHN Analyzer, ИК-спектроскопиче-ское исследование — на фурье-ИК-спектрометре Equinox 55 фирмы Bruker (Германия). Синтез смешанно--лигандного комплекса проводили с учетом полученных ранее данных исследования металл-ионных равновесий в данной системе [6]. Смешивали стехиометрические количества высокомолекулярного гепарина, раствора меди и глицина, устанавливая рН системы в интервале 6.80—7.20. После получасовой выдержки полученной смеси вводили охлажденный ацетон. С осадка геля сливали маточный раствор, а оставшийся гель высушивали. По данным элементного анализа, термогравиметрического анализа и ИК-спектроскопии был определен состав комплекса и предложена его брутто-формула: Na3CuHepGly • 2H2O. Как показал термический анализ полученного комплекса, процесс разложения является многостадийным и включает две стадии термической деструкции, о чем свидетельствуют перегибы на кривых потери массы. Потеря массы в температурном интервале 100—180°С указывает на отщепление кристаллизационной воды, присутствующей в комплексе. В данном случае в состав комплекса входят 2 молекулы воды.
Схема получения комплекса представлена ниже: Cu2+ +Hep^ + Cly— ^ CuHepCly3-.
Поглощение в области 3400 см-1 (рисунок) отвечает валентным колебаниям связи -О-Н. Полосы поглощения в области 3500-3300 см-1 соответствуют валентным колебаниям связи N-И в монозамещенной сульфамидной группе, но эти полосы перекрыты валентными колебаниями связи О-Н. Поглощение в области 2920 см-1 отвечает валентным асимметричным колебаниям связи С(алкильный) -Н в группе - СН2-, а в области 2850 см-1 - валентным симметричным. Полосу поглощения в области 1610 см-1 можно отнести к валентным асимметричным колебаниям связи С=О в карбоксилатной группе, а поглощение, отвечающее 1410 см-1, - к валентным симметричным колебаниям связи этой группы. Полосы поглощения в области 1230 и 1150 см-1 принадлежат асимметричным и симметричным валентным колебаниям связи O=S=O сульфамидной группы. Максимум, при ~1040 см-1 соответствует валентным асимметричным колебаниям связи С-О-С (простой эфир). Полосы поглощения в области 910 и 800 см-1 принадлежат асимметричным и симметричным валентным колебаниям связи S—O-C. Все максимумы, отвечающие значениям волнового числа до 1000 см-1, принадлежат области отпечатков пальцев и довольно трудны для идентификации. Здесь можно выделить деформационные колебания N-H при 700 см-1.
В таблице представлены спектральные характеристики гепарина и синтезированного комплекса гепарината меди с аминокислотой глицин.
ИК-спектроскопическое исследование комплекса показало изменения в области деформационных колебаний, которые свидетельствуют о том, что катион меди и аминокислота встраиваются в структуру гепарина (смещение полос поглощение функциональных групп -COOH, SO3, NSO3H).
Полученные результаты могут быть использованы для синтеза комбинированных препаратов, включающих молекулы двух и более типов, обладающих различным биологическим действием.
356
ФЕОФАНОВА и др.
Работа выполнена при финансовой поддержке Минобрнауки Российской Федерации в рамках выполнения государственных работ в сфере научной деятельности.
СПИСОК ЛИТЕРАТУРЫ
1. Карпухин Л.Е., Феофанова М.А., Николаева Л.С. и др. // Журн. неорган. химии. 2006. Т. 51. № 6. С. 979.
2. Николаева Л.С., Семенов А.Н., Мамонтов М.Н., Феофанова М.А. // Там же. 2009 . Т. 54. № 6. С. 1006.
3. Феофанова М.А., Францева Ю.В., Лапшин С.В. // Коорд. химия. 2012. Т. 38. № 5. С. 387.
4. Феофанова М.А., Францева Ю.В., Семенов А.Н., Баранова Н.В., Журавлев Е.В. // Журн. физ. химии. 2014.Т. 88. № 2. С. 361.
5. Видаль. Лекарственные препараты в России: Справочник. М.: Изд-во АстраФармСервис, 2003.
6. Николаева Л.С., Семёнов А.Н., Бурова Л.И. // Журн. неорган. химии. 2011. Т. 56. № 4. С. 689.
Для дальнейшего прочтения статьи необходимо приобрести полный текст. Статьи высылаются в формате PDF на указанную при оплате почту. Время доставки составляет менее 10 минут. Стоимость одной статьи — 150 рублей.