МАТЕРИАЛЫ КОНФЕРЕНЦИИ МОЛОДЫХ УЧЕНЫХ
В данной рубрике объединены несколько статей, материалы которых были представлены на V Конференции молодых ученых по общей и неорганической химии (14-17 апреля 2015 г. Москва, ИОНХ им. Н.С. Курнакова РАН)
УДК 546.04
ВЛИЯНИЕ СОЛЬВАТИРУЮЩЕЙ СПОСОБНОСТИ РАСТВОРИТЕЛЯ НА ПРОЦЕССЫ ФОРМИРОВАНИЯ АССОЦИИРОВАННЫХ СТРУКТУР ВОДОРАСТВОРИМЫХ Co(II) ФТАЛОЦИАНИНОВ © 2015 г. А. А. Воронина, А. А. Филиппова, С. А. Знойко, А. С. Вашурин, В. Е. Майзлиш
Ивановский государственный химико-технологический университет E-mail: asvashurin@mail.ru Поступила в редакцию 20.03.2015 г.
Изучены процессы самоассоциации сульфированных производных фталоцианина кобальта. Показано влияние размера периферического заместителя и сольватирующей способности среды на формирование H- и /-агрегатов металлофталоцианинов. Установлена возможность регулирования ассоциативного равновесия металлофталоцианинов за счет координационного взаимодействия с DABCO. Показано, что при введении DABCO в системе происходит диссоциация H- и /-агрегатов с дальнейшим образованием димеров сэндвичевого типа.
DOI: 10.7868/S0044457X15110239
Металлокомплексы фталоцианинов (MPc) проявляют уникальные каталитические [1—3], биохимические [4, 5] и фотохимические [6, 7] свойства. Широкие возможности химической модификации соединений данного класса (введение различных заместителей на периферию макромолекулы, расширение координационного центра, замена внутрициклических атомов азота на другие атомы, изменение центрального катиона металла) [8, 9] позволяют создавать жидкофазные системы и материалы с заданным набором физико-химических параметров [10, 11].
Особую роль при создании материалов на основе МРс и их дальнейшем функционировании играет сольватирующая способность среды (растворителя). В растворах металлофталоцианины формируют межмолекулярные ассоциаты за счет различного типа взаимодействий, включая универсальную и специфическую сольватацию [12, 13]. Растворитель при этом может вступать в пятое и шестое координационное положение металла [14] и выступать в качестве молекулярного регулятора строения димерных ассоциатов [15]. При переходе от растворов к кристаллосольватам [16, 17] состав и структура молекулярных комплексов МРс с растворителем и вид ассоциатов сохраняются. Тип агрегатов, а соответственно и физико-химические свойства супрамолекулярных систем, формирующихся на основе ассоциатов металлофталоцианинов, зависят от природы центрального катиона металла и периферических заместителей.
Сульфирование фталоцианинов не только придает им растворимость в водных средах, но и способствует усилению самоассоциации в растворах [18]. Между тем именно тетрасульфокис-лота фталоцианина кобальта нашла широкое применение в Мегох-процессе [19, 20]. Считается, что процессы самоассоциации тетрасульфо-фталоцианина кобальта снижают его каталитическую активность [21, 22].
Очевидно, что возможность управления ассоциативным состоянием водорастворимых МРс в
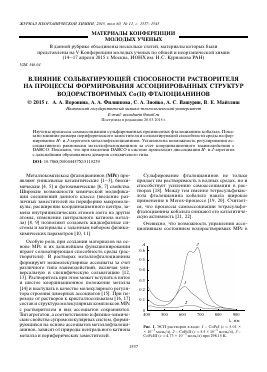
X, нм
Рис. 1. ЭСП растворов в воде: 1 — СоРс1 (с = 5.01 х х 10-5 моль/л), 2 - СоРс11 (с = 5.5 х 10-5 моль/л), 3 -СоРсШ (с = 4.73 х 10-5 моль/л) при 298.15 К.
1537
растворах открывает новые пути к созданию материалов на основе данных соединений. В настоящей работе предпринята попытка варьирования ассоциативного состояния МРс в растворах за счет процессов молекулярного комплексообразования.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Металлофталоцианины (СоРсГ—СоРсГУ) синтезированы из соответствующих фталодинитри-лов и очищены по известным методикам [23, 24].
SO3H
Растворители — ^^диметилформамид (ДМФА), диметилсульфоксид (ДМСО), пиридин (Py), ацетонитрил (An) — для проведения эксперимента подвергали очистке в соответствии с методиками, представленными в [25]. Перед использованием порцию растворителя подвергали фракционной перегонке.
Исследование процессов комплексообразова-ния проводили спектрофотометрическими методом. Электронные спектры поглощения (ЭСП) регистрировали в кварцевых кюветах на спектрофотометре Unico 2800 в спектральном диапазоне 300—900 нм. При проведении эксперимента ячейку термостатировали.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Растворимость металлофталоцианинов в воде достигается путем введения ионогенных группировок (сульфо- или карбоксигрупп) на периферию макромолекулы. Кроме универсальных взаимодействий большое влияние на этот процесс оказывает специфическая сольватация. На рис. 1 представлены ЭСП водных растворов СоРсГ, СоРсГГ и СоРсГГГ.
Вид ЭСП свидетельствует об ассоциированном состоянии металлофталоцианинов в воде и наличии в системе равновесия
(MPc)„
=>«MPc.
(1)
(a)
Рис. 2. Схема самоассоциатов СоРс в растворах: а — Д-агрегаты, б — /-агрегаты.
Таблица 1. Коэффициенты экстинкции (е) ассоциированных и мономерных форм растворенных металлофтало-цианинов
Макроцикл Растворитель ^м, нм еМ, л/(моль см) нм SD, л/(моль см) х 10-4, моль/л
СоРсГ* - - 615 4800 ± 50 1.54
СоРсГГ* Вода - - 630 800 ± 20 2.2
СоРсГГГ 678 32700±80 642 8930 ± 50 1.91
СоРсГУ Растворимость <1 мг/л
СоРсГГГ Ап—вода 676 18800±100 642 16400±90 5.60
СоРсГУ 678 12300±100 643 10800±70 4.54
СоРсГ 662 24200 ± 90 - - Мономер
СоРсГГ ДМФА 670 10400 ± 50 - - Мономер
СоРсГГГ 675 22350± 40 - - Мономер
СоРсГУ 675 13320±30 - - Мономер
СоРсГ 665 18850±60 - - Мономер
СоРсГГ ДМСО 664 2320 ± 20 - - Мономер
СоРсГГГ 675 24420 ± 40 - - Мономер
СоРсГУ 675 11900±20 - - Мономер
СоРсГ Не растворяется
СоРсГГ Пиридин
СоРсГГГ 668 7340 ± 20 - - Мономер
СоРсГУ 668 10510±20 - - Мономер
* Данные [28].
Анализ данных [26, 27] позволяет предположить, что при наличии в системе только универсальной сольватации ассоциация протекает с образованием Н- и /-агрегатов (рис. 2). Ранее нами было установлено [28], что ассоциированные формы сульфопроизводных металлофталоцианинов, у которых ионогенная группировка удалена от макроцикла нафтильными фрагментами (СоРсГ и СоРсГГ), имеют поглощение в области 620—630 нм, в то время как 0-полоса (мономерная форма) расположена в области 680—700 нм. В водной среде данные макроциклы формируют устойчивые Н-ас-социаты за счет перекрывания я-электронной плотности двух макроциклов. С увеличением количества ионогенных групп в периферическом заместителе степень димеризации, как правило, уменьшается. Константы диссоциации димеров СоРсГ и СоРсГГ представлены в табл. 1.
Введение нового структурного элемента периферического заместителя во фталоцианиновый
макроцикл способствует перераспределению электронной плотности в сопряженном макрокольце и способности МРс к формированию Н- и/или /-аге-рагатов. Для СоРсГГГ, содержащего триазольный фрагмент в составе периферического замещения, нами обнаружено усиление агрегации при стоянии водного раствора на свету в течение 5—6 ч. В ЭСП (рис. 3) наблюдается значительное уменьшение интенсивности поглощения в видимой области и изменение соотношения 0-полосы и полосы поглощения димерных форм. Равновесие (1) смещено влево.
С нашей точки зрения, это явление обусловлено кооперативным эффектом триазольного фрагмента и анионных групп в составе периферического заместителя, которые вызывают значительное нарушение распределения электронной плотности в сопряженном контуре макроцикла. Компенсация недостатка электронной плотности на центральном катионе металла происходит за счет образова-
A
X, нм
Рис. 3. Изменения в ЭСП водного раствора СоРсШ (с = 4.73 х 10-5 моль/л) при 298.15 К: 1 — исходный раствор, 2 — после выдерживания раствора в течение 5 ч на свету в закрытой кювете.
ния /-агрегатов, сформированных координационным взаимодействием нескольких макромолекул, которое схематично изображено на рис. 2. Кроме этого, стабилизация ассоциированной формы происходит за счет водородного связывания периферических заместителей одной макромолекулы с другой.
Низкая растворимость в воде (<1 мг/л) для СоРсГУ вероятнее всего, обусловлена слабой универсальной сольватирующей способностью воды по отношению к сильно ионизированной периферии фталоцианиновой макромолекулы и невозможностью специфического взаимодействия растворителя с триазольным фрагментом в составе периферического заместителя. Усиление сольватирующей способности воды по отношению к макроциклу СоРсГУ возможно путем перехода к бинарной системе растворителей с равной основностью, но с понижением кислотных свойств среды.
Растворимость СоРсГУ достигается в бинарном растворителе Ап—вода (1 : 1). Вода и ацето-нитрил имеют близкую основность: БЫ 18 и 14.1 [29, 30] соответственно, однако их кислотные свойства значительно различаются: АЫ 54.8 и 18.9 [29, 30] соответственно. Достаточная растворимость макроцикла в данном случае, вероятнее всего, обусловлена проявлением бинарной средой и универсальной, и специфической сольватации [31] как по отношению к ионогенной группе периферического заместителя, так и по отношению к триазольному фрагменту.
Для макроциклов СоРсГГГ и СоРсГУ при разбавлении бинарной смеси Ап—вода (рис. 4) в диапазоне концентраций от 4.78 х 10-4 до 1.63 х 10-5 моль/л интенсивность поглощения полосы ассоциированных форм и 0-полосы изменяется нелинейно,
что говорит о смещении равновесия (1). Изменение угла наклона кривой разбавления для раствора CoPcIII достигается при концентрации фтало-цианина 12.6 х 10-5 моль/л, для CoPdV — при концентрации макроцикла 16.93 х 10-5 моль/л. Далее разбавление подчиняется закону Ламбер-та—Бугера—Бэра на аналитических длинах волн. Наблюдаемая линейная зависимость оптической плотности при разбавлении растворов СоРсШ и CoPdV свидетельствует в пользу присутствия в растворе #-димеров, которые при диссоциации образуют мономерные формы. В случае формирования /-агрегатов соблюдение линейной зависимости ожидать не следует ввиду эффекта хромофорного влияния одной макроциклической молекулы на другую за счет координационного взаимодействия между ними.
Коэффициенты экстинкции (s) для #-агрега-тов представлены в табл. 1. Константы диссоциации димеров рассчитывали по уравнениям (2), (3) [32-34]:
Kdiss = 1/Kdim, (2)
- 4) = . (3)
= (2sM - Ед)(1 + 4Kdlll1|CoPc|) - (1 + 8Kdiin|CoPc| ).
8Kdim
Смещения ассоци
Для дальнейшего прочтения статьи необходимо приобрести полный текст. Статьи высылаются в формате PDF на указанную при оплате почту. Время доставки составляет менее 10 минут. Стоимость одной статьи — 150 рублей.