ХИМИЧЕСКАЯ ФИЗИКА, 2010, том 29, № 12, с. 40-49
ГОРЕНИЕ, ВЗРЫВ ^^^^^^^^^^^^ И УДАРНЫЕ ВОЛНЫ
УДК 541.126
МЕХАНИЗМЫ ОКИСЛЕНИЯ И ГОРЕНИЯ НОРМАЛЬНЫХ ПАРАФИНОВЫХ УГЛЕВОДОРОДОВ: ПЕРЕХОД ОТ Сх-С6 К С7Н16 © 2010 г. В. Я. Басевич*, А. А. Беляев, В. С. Посвянский, С. М. Фролов
Институт химической физики им. Н.Н. Семенова Российской академии наук, Москва
*Е-таП: basevich@center.chph.ras.ru Поступила в редакцию 24.05.2010
В работе применен предложенный ранее алгоритм построения оптимального механизма высоко- и низкотемпературного окисления и горения нормальных парафиновых углеводородов с главными процессами, определяющими скорость реакции и образование основных промежуточных и конечных продуктов. Механизм имеет статус неэмпирического детального, поскольку все элементарные реакции кинетически обоснованы. Две особенности характерны для этого механизма: в нем отсутствуют реакции так называемого двойного присоединения кислорода и не рассматриваются в качестве промежуточных частиц изомерные соединения и их производные. Применение упомянутого алгоритма приводит к достаточно компактным моделям, что важно при исследовании химических процессов с участием парафиновых углеводородов Сп с большим п. Ранее на основе такого алгоритма построены компактные механизмы окисления и горения пропана, н-бутана, н-пентана и н-гек-сана. В данной работе рассмотрен неэмпирический детальный механизм окисления и горения н-гептана. Важнейшая особенность нового механизма — проявление стадийности в виде холодных и голубых пламен при низкотемпературном самовоспламенении. Проведено сравнение результатов расчетов с экспериментальными данными.
Ключевые слова: углероды парафиновые С1—С7, окисление, горение, кинетика.
ВВЕДЕНИЕ
В последние годы для высших углеводородов предложены детальные механизмы их окисления и горения, включающие сотни частиц и тысячи элементарных химических актов. Такие механизмы учитывают многообразие промежуточных
стабильных молекул и радикалов в реакциях углеводородов. Например, в работе [1] для н-гептана представлена схема, содержащая 650 частиц и 2300 реакций, а в [2] — для н-декана — 715 частиц и 3872 реакций. Несмотря на неоспоримые достоинства таких детальных механизмов, их примене-
Р, отн. ед.
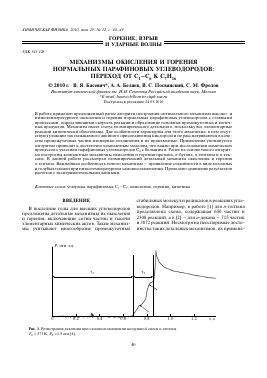
Рис. 1. Регистрация давления при самовоспламенении воздушной смеси н-гептана. Т0 = 573 К, Р0 =1.5 атм [4].
ние для решения многомерных задач газовой динамики горения затруднено в силу громоздкости. Вместе с тем, если учесть все возможные частицы-изомеры и реакции между всеми частицами, легко показать, что объемы механизмов в [1, 2] могут быть намного превзойдены (например, за счет включения полициклических ароматических углеводородов, сажи, фуллеренов, колебательно возбужденных молекул, реакций их образования и расходования и т.д.).
Кроме того, существует неопределенность в построении таких механизмов, поскольку отсутствуют многие необходимые и достаточно проверенные данные по термохимии и по скоростям реакций. Это сказывается на их кинетической обоснованности и точности.
Наконец, во всех известных публикациях отсутствует информация о применимости предлагаемых детальных кинетических механизмов к описанию многостадийного низкотемпературного окисления углеводородов [3], сопровождаемого образованием не только холодных, но и голубых пламен [4, 5]. В монографии [3] и статьях [4, 5] приводятся экспериментальные регистрации давления в закрытом сосуде при многостадийном самовоспламенении смесей изооктана и я-гептана с воздухом. На кривой изменения давления (рис. 1) можно отчетливо выделить три стадии самовоспламенения: первая — холодное пламя с задержкой т1, вторая — голубое пламя и третья — горячий взрыв. Продолжительность первой и второй стадий (указаны стрелками) соответствует задержке горячего взрыва и отмечена как т2 (авторы работы [4] дают другое объяснение этим эффектам, но в публикации [3] уже вводится концепция много-стадийности). Суммарная задержка самовоспламенения
Т = Т1 + Т2.
Указанные эффекты не только реально существуют, но и играют важную роль, например в предпламенных процессах в поршневых двигателях внутреннего сгорания, поэтому детальные кинетические механизмы окисления углеводородов, несомненно, должны их воспроизводить, а также описывать чувствительность к внешним условиям.
Известные детальные кинетические механизмы, как правило, не являются всеобъемлющими и в определенной степени ограничены. Между тем для решения конкретных задач, в которых должны быть учтены главные процессы, определяющие скорость реакции и образование основных промежуточных и конечных продуктов, представляют интерес не максимальные, а оптимальные механизмы окисления и горения углеводородов. Такие механизмы, даже если они достаточно компактны, не теряют статуса неэмпирических детальных механизмов, пока все
2100 1800 1500 1200 900 600
т, К
1.2 1.3 1.4 1.5 1.6 1.7
г, с
Рис. 2. Расчетная зависимость температуры от времени при самовоспламенении стехиометрической смеси 1.86 об. % С7Н!б~воздух: Т0 = 573 К, Р0 = 1.5 атм.
составляющие их элементарные реакции имеют кинетическое обоснование. Другими словами, при моделировании окисления и горения углеводородов всегда имеется возможность неэкстенсивного построения механизмов с целевым ограничением многообразия продуктов и реакций, но с сохранением основных каналов процесса и принципиально важных типов элементарных актов.
Известна общность в феноменологическом описании реакций парафиновых углеводородов [3—5]. Это позволяет применить алгоритм, рассмотренный в работах [6—9] и использованный ранее для построения химического механизма окисления и горения парафиновых углеводородов (от пропана до я-гексана), для построения механизма окисления и горения следующего члена гомологического ряда — я-гептана. В алгоритм [6—9] заложен принцип неэкстенсивного построения механизма, основанный на следующих допущениях: низкотемпературное разветвление описывается группой реакций с одним присоединением кислорода; каналы реакций окисления через изомерные формы можно исключить из рассмотрения, поскольку они медленнее, чем окисление через не-изомеризованные частицы. Подчеркнем, что механизмы окисления С7Н16 неоднократно предлагали ранее (см., например, [10, 11]), однако, как и в упомянутых выше случаях, не было показано, что эти механизмы адекватно описывают многостадийное окисление углеводородов с образованием не только холодных, но и голубых пламен при самовоспламенении. Построение оптимального механизма окисления С7Н16, основанного на принципе неэкстенсивности и проявляющего стадийность в виде холодных и голубых пламен при низкотемпературном самовоспламенении,
^ (ъ, С)
-0.5
-1.5
-2.5
-3.5
-4.5
0.6
Р - 2.8 атм
4.5
13-15
3.2
40
о
1.0
1.2
1.4
1.6 1.8 1000/ т, к
Рис. 3. Зависимости задержек самовоспламенения от температуры для стехиометрической смеси 1.86 об. % СуН^—воз-дух при давлении Ро — 2.8-40 атм: Точки — опыты [12-18], кривые — расчет.
необходимо и важно для получения оптимальных механизмов окисления более сложных углеводородов — СпН2п + 2 при п > 7.
ПОСТРОЕНИЕ МЕХАНИЗМА
Согласно алгоритму [6—9], при разработке кинетического механизма углеводорода СпН2п + 2 за основу берется механизм его аналога в гомологическом ряду с числом атомов углерода п, меньшим на единицу — С(п — 1)Н2(п — ^ + 2. Это относится и к реагентам и к реакциям. В гомологическом ряду аналогом, предшествующим я-гептану является я-гексан, поэтому за основу взят механизм окисления и горения С1—С6, включающий 72 частицы и 499 реакций [9]. В дополнение к механизму окисления я-гексана в кинетический механизм для я-гептана потребовалось ввести 9 новых частиц и 124 элементарных акта, так что полученный механизм в целом включает 81 частицу и 623 реакции. Алгоритм [6—9] реализован в виде вычислительной программы, которая отбирает новые частицы, новые реакции и их аррениусовские параметры. Дополнительные
частицы с энтальпиями образования АН^98, эн-
тропией S%98 и теплоемкостями при постоянном давлении
с
- с + сТ + сТ р - С0 + 103 +
2
+ -
сТТ
10° 109
а также дополнительные реакции и их аррениу-совские параметры представлены в табл. 1 и 2.
Возникновение холодного и голубого пламени при многостадийном самовоспламенении — характерный пример критических явлений в химической кинетике. Известно, что критические явления многофункциональны и проявляются при определенном соотношении скоростей разных элементарных стадий. Поэтому при их кинетическом моделировании требуются дополнительный анализ и подбор констант скоростей важнейших реакций в диапазоне теоретически допустимых значений, не превосходящих экспериментальные погрешности. Другими словами, простая подстановка приближенных значений определяющих констант скоростей не всегда позволяет описать наблюдаемые критические явления. Для полученного механизма окисления я-гептана такая корректировка констант потребовалась применительно к ограниченному числу процессов — реакций я-гептана с гидропероксидными радикала-
Таблица 1. Реагенты, включенные в механизм окисления и горения и-гептана
№ Реагент кал/моль °298, кал/(моль ■ К) кал/(моль ■ К) с1, 2 кал/(моль ■ К2) с2, 3 кал/(моль ■ К3) c3, 4 кал/(моль ■ К4)
73 С7Н16 -0.445Е+05 0.103Е+03 0.431Е+00 0. 159Е+03 -0.862Е+02 0.182Е+02
74 С7Н15 0.367Е+04 0.106Е+03 0.207Е+01 0. 150Е+03 -0.840Е+02 0.207Е+02
75 С7Н15О2 -0.240Е+05 0.125Е+03 0.290Е+01 0. 175Е+03 -0.106Е+03 0.294Е+02
76 С7Н15О2Н -0.597Е+05 0.123Е+03 0.258Е+01 0 178Е+03 -0.106Е+03 0.288Е+02
77 С7Н15О -0.262Е+05 0.116Е+03 0.178Е+00 0. 175Е+03 -0.107Е+03 0.315Е+02
78 С6Н13СНО -0.649Е+05 0.111Е+03 0.112Е+02 0. 110Е+03 -0.678Е+01 -0.351Е+02
79 С7Н13СО -0.297Е+05 0.112Е+03 0.112Е+02 0. 110Е+03 -0.678Е+01 -0.351Е+02
80 С7Н14 -0.148Е+05 0.102Е+03 0.237Е+01 0. 142Е+03 -0.760Е+02 0.158Е+02
81 С7Н13 0.293Е+05 0.101Е+03 0.298Е+01 0. 128Е+03 -0.648Е+02 0.127Е+02
ми и реакции гептанового радикала с молекулярным кислородом.
ПРОВЕРКА МЕХАНИЗМА Опыты по самовоспламеиеиию газовых смесей
Предсказательную способность механизма проверили, сравнив результаты расчетов с известными эксперименталь
Для дальнейшего прочтения статьи необходимо приобрести полный текст. Статьи высылаются в формате PDF на указанную при оплате почту. Время доставки составляет менее 10 минут. Стоимость одной статьи — 150 рублей.