НЕОРГАНИЧЕСКИЕ МАТЕРИАЛЫ, 2012, том 48, № 1, с. 57-59
УДК 536.63
ВЫСОКОТЕМПЕРАТУРНАЯ ТЕПЛОЕМКОСТЬ Pb2SnO4 © 2012 г. В. М. Денисов, В. П. Жереб, Л. Т. Денисова, Л. А. Иртюго, С. Д. Кирик
Институт цветных металлов и материаловедения СФУ, Красноярск e-mail: antluba@mail.ru Поступила в редакцию 07.07.2011 г.
В интервале 500—1000 K измерена теплоемкость Pb2SnO4. По экспериментальным данным рассчитаны термодинамические функции твердого оксидного соединения.
ВВЕДЕНИЕ
Изучение теплофизических параметров оксидных соединений на основе РЬО имеет как научное, так и прикладное значение в связи с их важными свойствами [1].
Диаграмма состояния системы РЬО—8пО2 характеризуется наличием одного соединения РЬ28пО4, которое плавится с разложением при 1333 К [2—4]. Есть данные о том, что при взаимодействии в системе РЬО—8пО2 может образоваться и соединение РЬ8пО3 в присутствии в качестве стабилизатора 8Ю2 [2, 3]. Согласно [3], синтез РЬ8пО3 в мономинеральном виде возможен только в условиях высоких температур и давлений.
I
Цель данной работы — измерение высокотемпературной теплоемкости и определение по этим данным термодинамических свойств Pb2SnO4.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
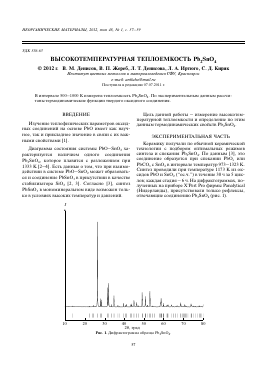
Керамику получали по обычной керамической технологии с подбором оптимальных режимов синтеза и спекания Pb2SnO4. По данным [3], это соединение образуется при спекании PbOx или PbCO3 с SnO2 в интервале температур 973—1323 K. Синтез проводили при температуре 1173 K из оксидов PbO и SnO2 ("ос.ч.") в течение 30 ч за 5 циклов; каждая стадия — 6 ч. На дифрактограммах, полученных на приборе X'Pert Pro фирмы Panalytical (Нидерланды), присутствовали только рефлексы, отвечающие соединению Pb2SnO4 (рис. 1).
10
20
30
60
40 50
29,град
Рис. 1. Дифрактограмма образца Pb2SnO4.
70
80
58
ДЕНИСОВ и др.
196 г
192 -
а
л §
Üfr
188 -
184 -
180
176
Теплоемкость и термодинамические функции Pb2SnO4
500 600 700 800 900 1000 1100 T, K
Рис. 2. Температурная зависимость теплоемкости Pb2SnO4.
Теплоемкость (Cp) измеряли в платиновых тиглях методом дифференциальной сканирующей калориметрии на приборе STA 449 C Jupiter (NETSCH). Методика измерений описана нами в [5, 6].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Температурная зависимость Cp Pb2SnO4 показана на рис. 2. Видно, что в измеренном интервале температур значения Cp закономерно увеличиваются, а на зависимости Cp(T) нет различного рода экстремумов. Сглаженные значения Cp(T) могут быть описаны соотношением
Cp = 155.27 + 38.1 х 10-3T +
+ 6.5 х 10T2 (Дж/(моль K)).
Это позволяет определить №(T) — №(500 K) и S°(T) — S0(500 K) по известным термодинамическим уравнениям. Результаты расчета приведены в таблице.
Для системы PbO—GeO2 в [5] установлено, что
между удельной теплоемкостью (C° ) и составом
оксидов имеется корреляция: значения Cp закономерно убывают по мере роста содержания PbO. Данное явление согласуется с эффектом атомных масс: фононные частоты лежат ниже для оксидов с высоким содержанием PbO. Это приводит к уменьшению температуры Дебая и, соответственно, теплоемкости оксидов с более высоким содержанием тяжелых атомов.
С использованием величин CР для SnO2 и PbO [7], а также рассчитанных нами по уравнению зависимости Cp(T) значения C° для Pb2SnO4 получена подобная корреляция и для системы PbO—
Т, K Cp, Дж/(моль K) №°(7) - №°(500 K), Дж/моль S°(T) - S°(500 K), Дж/(моль K)
510 177.23 1719.9 3.51
520 177.52 3444.6 6.95
530 177.81 5174.0 10.33
540 178.10 6908.1 13.65
550 178.40 8646.9 16.92
560 178.71 10390 20.14
570 179.02 12138 23.30
580 179.33 13890 26.42
590 179.65 15647 29.48
600 179.97 17409 32.50
610 180.29 19174 35.48
620 180.61 20945 38.41
630 180.94 22719 41.30
640 181.27 24498 44.15
650 181.60 26281 46.96
660 181.94 28068 49.74
670 182.28 29860 52.48
680 182.61 31656 55.18
690 182.95 33456 57.84
700 183.30 35260 60.48
710 183.64 37068 63.08
720 183.99 38882 65.65
730 184.33 40698 68.19
740 184.68 42520 70.70
750 185.03 44345 73.18
760 185.38 46174 75.63
770 185.73 48007 78.05
780 186.09 49845 80.45
790 186.44 51 686 82.82
800 186.80 53532 85.17
810 187.15 55381 87.49
820 187.51 57235 89.79
830 187.87 59093 92.06
840 188.23 60955 94.31
850 188.59 62820 96.54
860 188.95 64690 98.75
870 189.31 66564 100.9
880 189.67 68442 103.1
890 190.03 70320 105.2
900 190.39 72210 107.4
910 190.76 74100 109.5
920 191.12 76000 111.5
930 191.48 77890 113.6
940 191.85 79790 115.7
950 192.22 81 700 117.7
960 192.58 83610 119.7
970 192.95 85520 121.7
980 193.32 87440 123.7
990 193.68 89360 125.6
1000 194.05 91290 127.6
ВЫСОКОТЕМПЕРАТУРНАЯ ТЕПЛОЕМКОСТЬ Pb2SnO4
59
SnO2: значения Cp уменьшаются при изменении состава от SnO2 к PbO.
СПИСОК ЛИТЕРАТУРЫ
1. Курзина И.А., Галанов С.И., Курина Л.Н. Фазовый состав оксидной свинец—оловянной системы // Журн. прикл. химии. 2002. Т. 75. № 1. С. 6—9.
2. Торопов Н.А., Барзаковский В.П., Лапин В.В. и др. Диаграммы состояния силикатных систем: Справочник. Вып. 1. Двойные системы. Л.: Наука, 1969. 822 с.
3. Диаграммы состояния систем тугоплавких оксидов: Справочник. Вып. 5. Двойные системы. Ч. 1 / Под ред. Галахова Ф.П. Л.: Наука, 1985. 284 с.
4. Уразов Г.Г., Сперанская Е.И., Гуляницкая З.Ф. Физико-химическое изучение взаимодействия окиси свинца с оксидами сурьмы и олова // Журн. неорган. химии. 1956. Т. 1. № 6. С. 1413-1417.
5. Денисов В.М., Иртюго Л.А., Денисова Л.Т. Высокотемпературная теплоемкость оксидов системы GeO2-PbO // ФТТ. 2011. Т. 53. № 4. С. 642-646.
6. Денисова Л.Т., Иртюго Л.А., Денисов В.М., Би-ронт В.С. Теплоемкость, теплопроводность и термическое расширение монокристаллов Bi12SiO20 // Журн. СФУ. Техника и технологии. 2010. Т. 3. № 2. С. 214-219.
7. Физико-химические свойства окислов: Справочник / Под ред. Самсонова Г.В. М.: Металлургия, 1978. 472 с.
Для дальнейшего прочтения статьи необходимо приобрести полный текст. Статьи высылаются в формате PDF на указанную при оплате почту. Время доставки составляет менее 10 минут. Стоимость одной статьи — 150 рублей.